정의: 기체 상태에서 결합 1 mol을 끊는데 (균일 분해에) 필요한 에너지 혹은 엔탈피 변화를 뜻한다. ex) H2 (g) → 2H(g)
결합 에너지(BDE, D0,)는 공유결합분자의 공유결합세기를 비교하는 기준점이 되기 때문에 기본 개념을 확립해야 하며 격자에너지와 관계없는 개념이라는 것을 인지해야 한다.
- 흡열반응 (+ΔH) 이다.
- 결합에너지의 엔탈피 변화 (반응열 계산): ΔH = 반응물의 결합 에너지의 합 - 생성물의 결합 에너지의 합
- 결합 에너지의 Trends ★
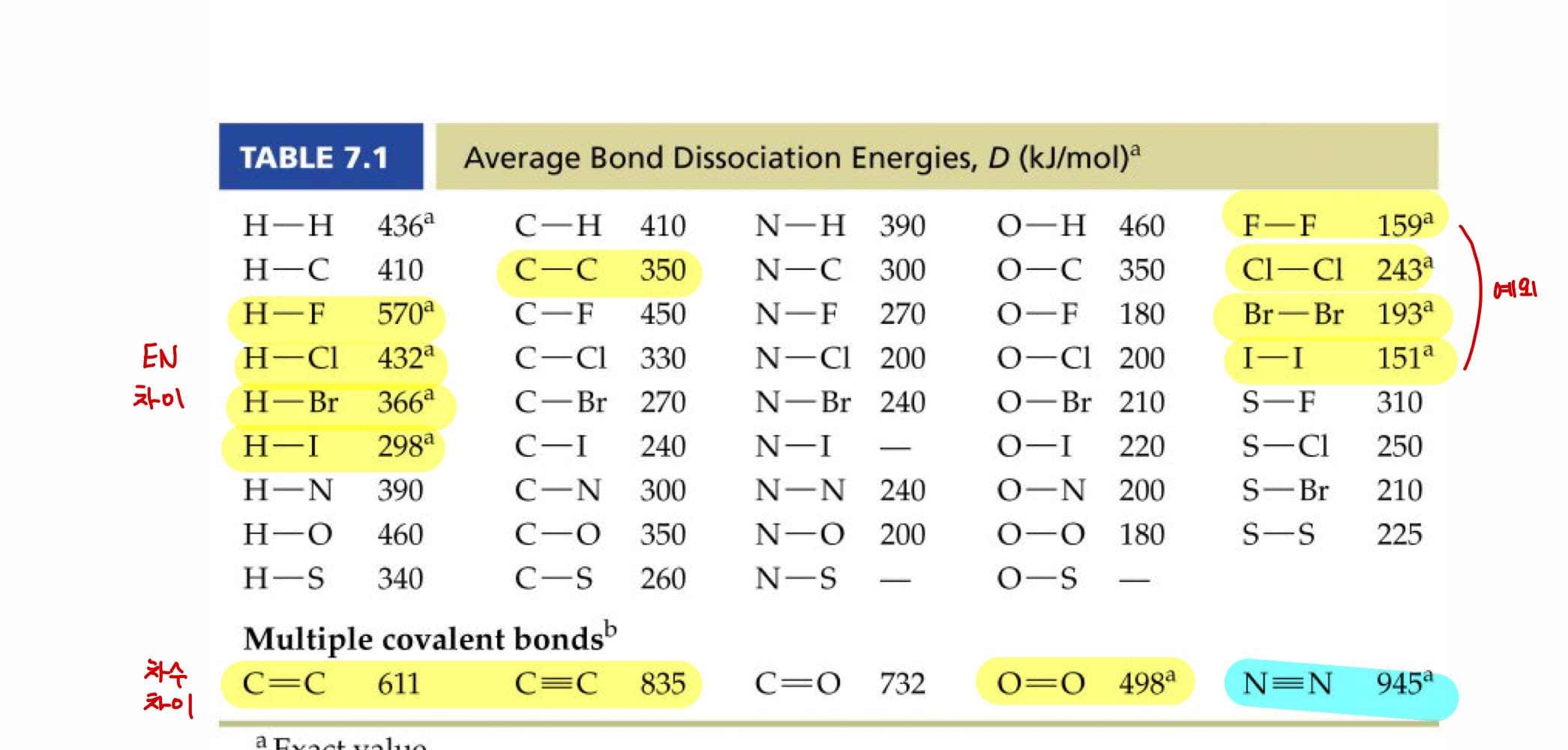
- 아래 표를 참고하자. 기본적으로 결합 길이와 결합 에너지는 반비례한다는 것을 기저로 깔로 각 개념을 이해해 보자
| 핵-공유전자쌍 간의 거리 (유효 핵전하) ↓ | 유효 핵전하가 커지면 전자를 당겨오는 힘또한 커지기 때문에 원자 반지름이 줄어들고 이로힌해 결합 길이가 감소한다. | 결합에너지 증가 |
| 비공유 전자쌍의 개수 ↓ | 결합에너지 증가 | |
| 전기 음성도의 차이 ↑ (극성의 유무가 아님) | 전기 음성도가 커지면 dipole moment가 커지면서 EN이 큰 원소가 전자 공유쌍을 더 강하게 가져오게된다. | 결합에너지 증가 |
| 결합차수 ↑ | 단일 결합은 1차 이중 결합은 2차 이런식으로 간단하게 볼수있지만 MO 이론에서는 계산하는 방법이 다르니 반드시 참고 | 결합에너지 증가 |
| 중심원자의 산화수 ↑ | 결합에너지 증가 |
- 추가적인 팁
- N2 삼중결합이 결합해리 에너지의 최댓값 (945 kJ/mol)
- 유일한 예외가 있는데 그게 Cl2 > Br2 > F2 > I2인데 일반적인 트렌드로 추측이 안되고 그냥 암기해야 한다. 당연히 문제에서도 자주 출제된다.
반응형
'일반화학 > 화학기초' 카테고리의 다른 글
| 세기 성질 (intensive property) vs 크기 성질 (extensive property) (0) | 2023.02.09 |
|---|---|
| 전자쌍 반발 이론 (VSEPR Theory) ☆ (0) | 2022.09.25 |
| 원소의 주기성 2 ★ - 전자 친화도/전기 음성도 (1) | 2022.09.20 |
| 원소의 주기성 1 ★ (0) | 2022.09.19 |



댓글