일반 화학 범위내에서 시험문제가 나온다면 항상 빠지지 않고 등장하는 주제이다.
그리 난이도가 높은 문제는 아니지만, 저번 포스터에 작성한 분자간의 힘의 개념이 확실히 암기되어 있지 않다면 헷갈리기 쉽다.
오늘은 문제들을 예시로 하여 설명할 건데 그 전에 꼭 암기해야 할 것이 있다.
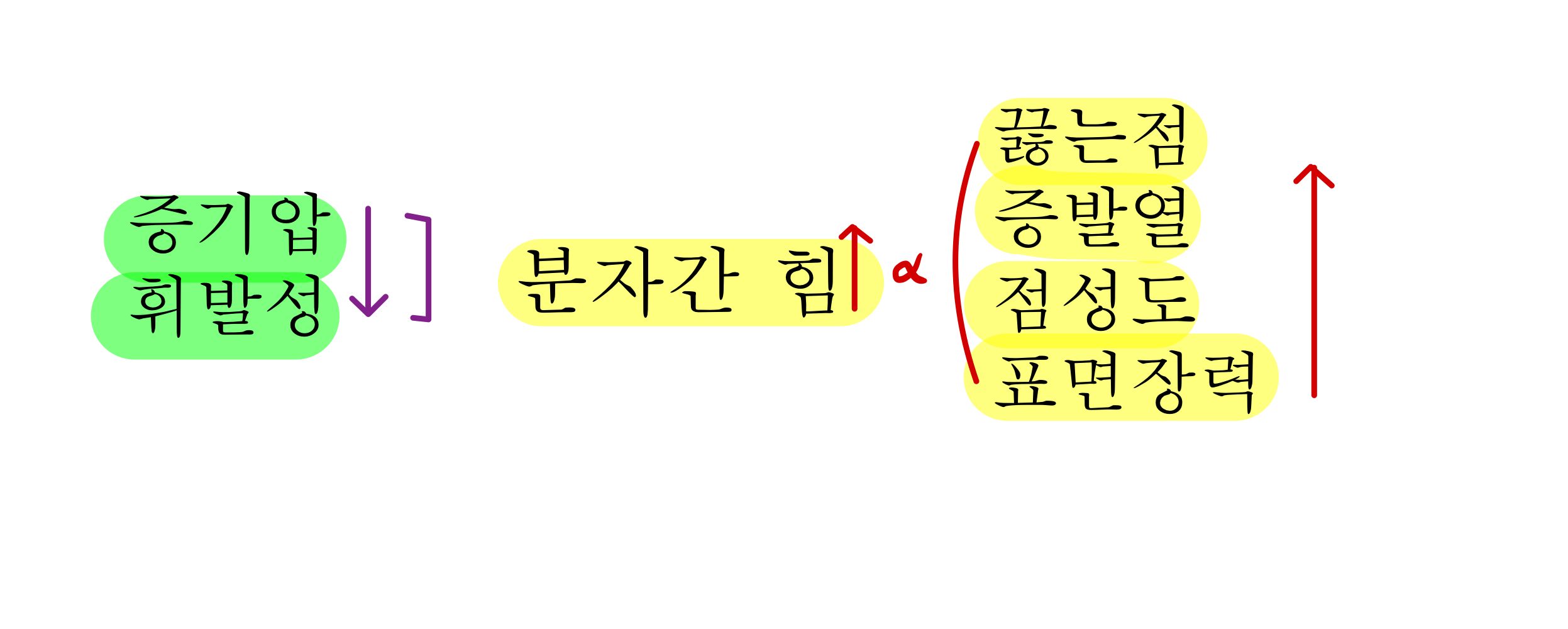
사진에서 표현된 각 성질들과의 비례관계를 확실히 암기하는것은 선택이 아닌 필수니 무조건 암기하자.
- ex 1) 다음 일원자분자 중 끓는점이 가장 높은 것은?
- a) He b) Ar c) Ne d) Kr
- ex 2) 끓는 점이 큰 순서대로 나열하라
- H₂O, H₂S, H₂Te, H₂Se
- ex 3) CH₄ 과 SO₂ 중에서 증발열이 더 큰 것을 고르고 어떠한 분자간의 힘이 적용됬는지 적어라
- ex 4) 끓는점의 크기가 올바르게 나열된것은?
- a: H₂O b: CH₃Cl c: Hg d: HF
- a) a > c > d > b
- b) c > a > d > b
- c) c > d > a > b
- ex 5) 아래의 분자들을 끓는점이 커지는 순서대로 나열하라
- CH₃CH₂CH₂CH₃, CH₃CH₂CH₂OH, CH₃CH₂OCH₂CH₃, HOCH₂CH₂OH
- ex 1) 다음 일원자분자 중 끓는점이 가장 높은 것은?
- a) He b) Ar c) Ne d) Kr
- noble gas 를 비교하는 문제이다. 같은 족 원소를 비교하고 있으며 아래로 갈수록 분자량이 커진다. 그럼므로 가장 무거운 Kr의 끓는 점이 가장 높다
- ex 2) 끓는 점이 큰 순서대로 나열하라
- H₂O, H₂S, H₂Te, H₂Se
- H₂O > H₂Te > H₂Se > H₂S
- H₂O은 4개의 분자 중 유일하게 수소결합을 한다. 즉 분자간 힘이 가장 세고. 나머지는 분자량으로 비교하면 되는데
- 분자량 크기 비교를 하면 Te > Se > S 순이기 때문에 이 트렌드를 그대로 적용하면 위 같은 답이 나온다.
- ex 3) CH₄ 과 SO₂ 중에서 증발열이 더 큰 것을 고르고 어떠한 분자간의 힘이 적용됬는지 적어라
- CH₄: 분산력
- SO₂: 쌍극자
- SO₂는 극성분자이고 쌍극자 모멘트가 0이 아님으로 분자간의 힘이 더 세고 증발열 또한 CH₄ 보다 강하다
- ex 4) 끓는점의 크기가 올바르게 나열된것은?
- a: H₂O b: CH₃Cl c: Hg d: HF
- a) a > c > d > b
- b) c > a > d > b
- c) c > d > a > b
- 금속결합이 분자간 힘보다 끓는점이 훨씬 높다. 그럼으로 금속( 양이온 + 자유전자) 이 수소결합 보다 강하고 수소결합이 쌍극자 보다 강하다
- 이전 글에 설명했듯 더 많은 수소결합을 하는 물이 HF 보다 끓는점이 높다. 이해가 안가면 그냥 외워도 된다.
- ex 5) 아래의 분자들을 끓는점이 커지는 순서대로 나열하라
- CH₃CH₂CH₂CH₃, CH₃CH₂CH₂OH, CH₃CH₂OCH₂CH₃, HOCH₂CH₂OH
- CH₃CH₂CH₂CH₃ < CH₃CH₂OCH₂CH₃ < CH₃CH₂CH₂OH < HOCH₂CH₂OH
- CH₃CH₂OCH₂CH₃ 분자내 산소가 있지만 이 녀석은 수소결합을 하지 못한다. 왜냐면 산소에 H 가 붙어있지 않기 때문이다. 하지만 CH₃CH₂CH₂CH₃ 보다는 분자량이 크기에 끓는점이 더 높다
- CH₃CH₂CH₂OH < HOCH₂CH₂OH 는 간단하게 그냥 HOCH₂CH₂OH가 줄수 있는 H가 더 많고, 즉 더 많은 수소결합이 가능하기에 끓는점이 높다.

반응형
'일반화학 > 액체, 고체, 기체' 카테고리의 다른 글
| 고체의 결정 구조 (단순, 체심, 면심) ★ (0) | 2023.09.19 |
|---|---|
| 분자간 힘 - 수소 결합, London forces ★ (0) | 2022.08.24 |


댓글