갈바니 전지는 볼타 전지라고도 하며 초기 전지 모델이다.
1. 볼타 전지
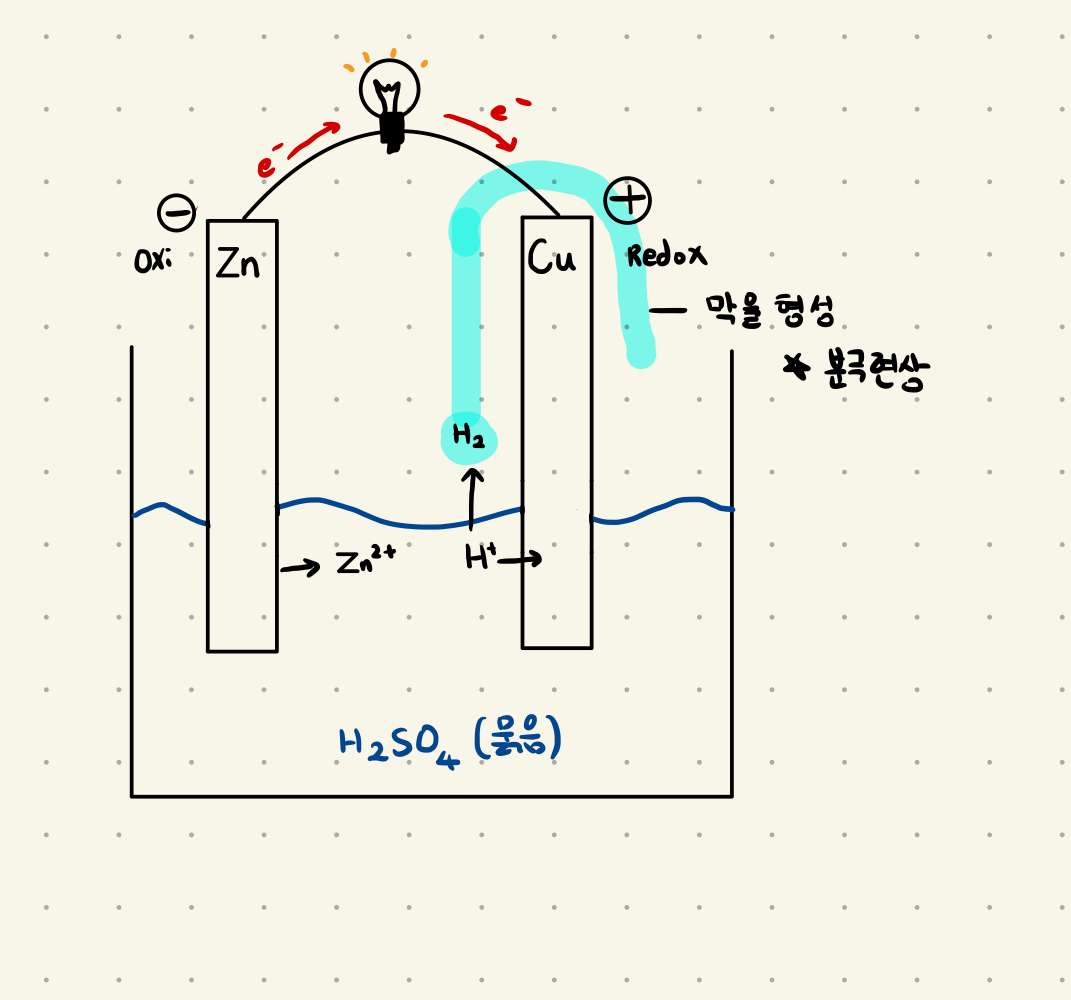
- 묽은 황산이 담긴 하나의 비커에 Zn 판과 Cu 판을 담궈 이를 도선으로 연결해 만든 전지
- 각 전극에서의 반응
- 전지의 표시: Zn(s) ㅣ H2SO4(aq) ㅣ Cu (s) E˚ = 1.1 V
- 양극 Anode: Zn (s) ⇌ Zn2+(aq) + 2e-
- 음극 Cathode: 2H+(aq) + 2e- ⇌ H2(g)
- 개념정리 (암기) ★
| 전극의 종류 (Anode and Cathode) | 갈바니 전지 |
| 양극 | 산화반응이 일어나는곳 - (negativie) 극 전자를 생성 염다리의 음이온이 이동하는 극 |
| 음극 | 환원반응이 일어나는 곳 + (positive) 극 전자를 받음 염다리의 양이온이 이동하는 극 |
- Zn의 질량감소 ★
- 분극현상: 볼타전지는 H2 기체에 의한 분극현상에 의해 효율이 떨어졌는데, 분극 현상이란 H2기체가 Cu 판 주위에 막을 형성하여 전류의 흐름을 막는 현상이다.
- 이를 극복하기위한 감극제 (산화제) 가 사용되었다. (ex. MnO2, H2O2)
2. 다니엘 전지
- 다니엘 전지는 각판을 다른 비커에 두고 각각 ZnSO4 와 CuSO4 수용액을 채워넣어 도선으로 연결후 "염다리(salt bridge)" 를 연결했다.
- 이 염다리는 이온통로 역활을 하는데 반응이 진행되는 동안 각 격실의 용액의 전기적 중성 (알짜 전하 0) 을 유지시켜준다.
- 음이온은 양극으로 이동하고 양이온은 음극으로 이동하는 식으로 전기적 중성을 유지하며 안정적인 전지를 구성할수 있었다.
- 각 전극에서의 반응
- Zn(s) ㅣ Zn2+(aq) II Cu2+(aq) ㅣ Cu (s) E˚ = 1.1 V
- 양극 Anode: Zn (s) ⇌ Zn2+(aq) + 2e-
- 음극 Cathode: Cu2+(aq) + 2e- ⇌ Cu(s)
- Zn 질량 감소, Cu 질량증가 ★

개념정리할때 양극과 음극의 차이 각 전지의 판의 질량 감소 및 증가를 확실히 구분하면 좋을거 같다.
*추가 내용
- 전자 (eletron)은 항상 양극에서 음극으로 향한다.
- 갈바니 전지는 자발적인 반응이며 기전력은 양수이다.
- 전지 반응은 평형상태에 도달할때까지 진행된다
반응형
'일반화학 > 전기화학' 카테고리의 다른 글
| 다음 중 산화-환원 반응이 아닌것은..? (0) | 2023.09.13 |
|---|---|
| 화학 반응식 균형 맞추기 ★ (0) | 2022.09.28 |
| 배터리 종류 (0) | 2022.09.16 |
| 선 표시법 Cell Diagram (0) | 2022.09.15 |
| 산화 - 환원 반응(Oxidation-Reduction Reactions) - ★ (2) | 2022.09.13 |



댓글