1. 리간드 세기
I- < Br- < Cl- < OH- < F- < H₂O < NH₃ < en < NO₂- < CN- < CO
- 왼쪽부터 약한 장 리간드 (Weak-field ligand) 오른쪽 CN- 와 CO는 강한 장 리간드이다. (Strong-field ligand)
- 약한 장 리간드 = Δ(결정장 갈라짐) ↓ ; 강한 장 리간드 = Δ ↑
2. High spin vs Low spin
a) 팔면체: 배위수 6; Low and High 모두 가능함 (*4주기 전이원소가 가능함, 5~6주기 전이금속은 보통 저스핀임)
- Δ > P; 저스핀, 강한 장 리간드와 결합했을때
- P 짝지음 에너지, 페어링 에너지, 전자쌍 반발 등등으로 불림
- Δ < P; 고스핀, 약한 장 리간드와 결합했을때
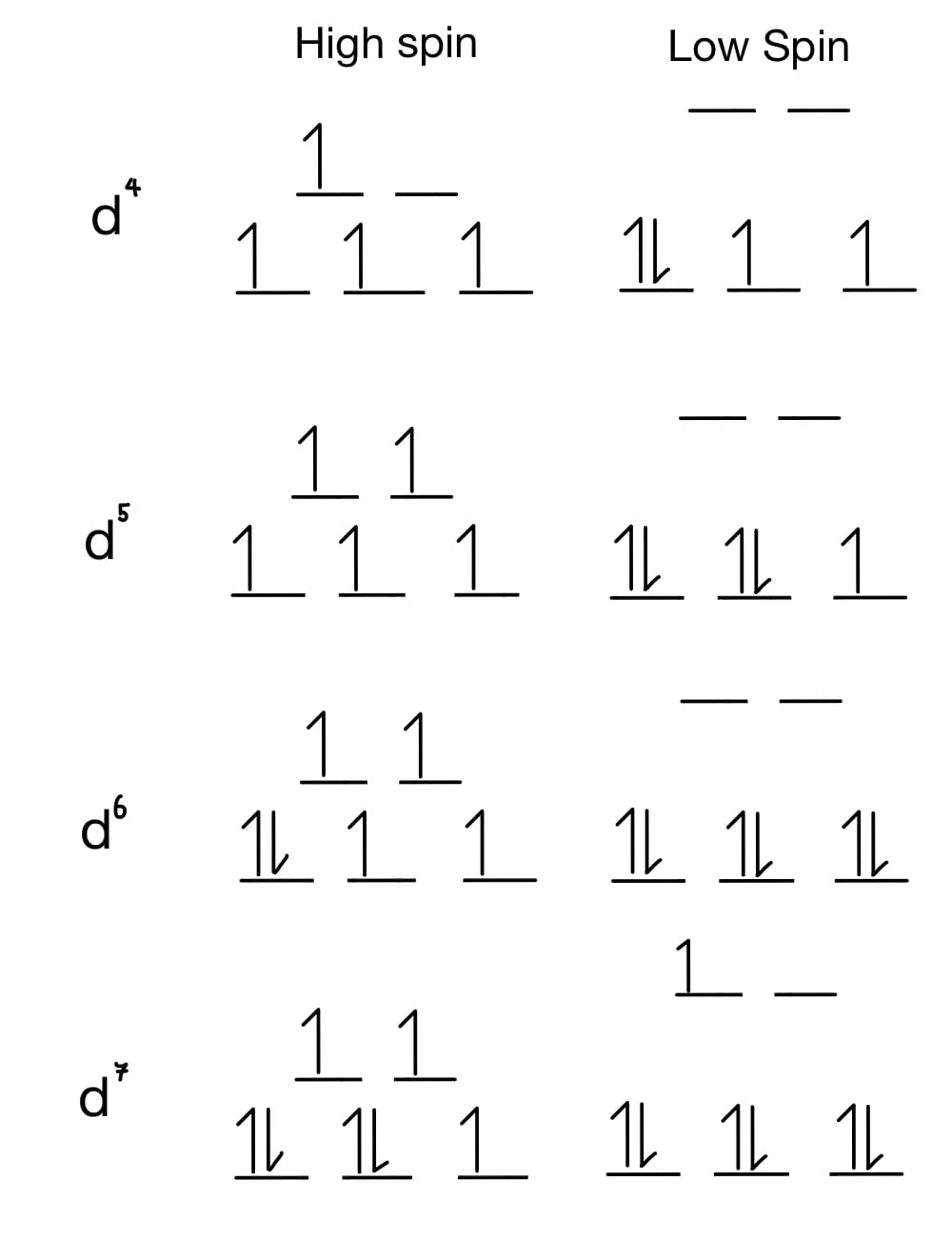
- 다음과 같은 전자배치를 가지는 금속이온은 저스핀과 고스핀에서 홀전자 (스핀)의 수는 동일하다 d1 ~ d3, d8 ~ d10
- d4 ~7 은 고스핀과 저스핀의 홀전자 수가 다르다. 주어진 착물이 상자기성인지 반자기성인지 판단할수 있음
b) 정사면체: 배위수 4개; 오직 high spin
- 정사면체의 경우 리간드가 축 사이로 들어와서 오비탈과 가깝고 그로인해 반발이 강해 P값이 높음= 고스핀만 가능
- Δ < P
- 팔면체의 Δ = 사면체의 4/9Δ
- 팔면체의 반대의 배열을 가진다.

c) 평면 사각형: 배위수 4개; 오직 low spin
- 리간드가 x,y축으로 접근함

d) 선형: 리간드 2개; 일부 금속이온만 가능함 (Ag+, Au+, Cu+)
- 리간드가 z 축으로 접근함

각 팔면체,평면 사각형, 정사면체의 오비탈의 위치를 꼭 암기해야함. (높은 수록 에너지 큼)
반응형
'일반화학 > 배위화학' 카테고리의 다른 글
| 결정장 이론 - 색 (0) | 2022.10.21 |
|---|---|
| 평면 사각형/정사면체를 이루는 전이금속 (배위화학) (0) | 2022.10.12 |
| 배위화합물의 명명법 (Nomenclature of coordination compound) (0) | 2022.10.09 |
| 리간드의 종류 (Types of Ligand) 와 배위수 ★ (0) | 2022.10.08 |


댓글